关键要点
- 同一 RIN 编号下,数日内出现两场 EO 12866 审查会议申请。
- 指南草案旨在明确调味 ENDS 在 APPH 法定框架下的证据标准。
- Breeze 在 2025 年 FDA 执法强化后收入下降约 90%。
- Glas 由顶级 FDA 监管律所代理参与行政审查程序。
- FDA 于 2026 年 2 月 18 日将草案提交 OIRA 启动跨部门审查。
- OIRA 审查监管分析与经济影响,但不替代 FDA 科学判断。
- 指南最终文本或进一步界定调味 ENDS 的现实授权路径。
2Firsts, 2026年3月3日
美国监管信息网(RegInfo.gov)显示,在同一监管编号 RIN 0910-ZC78 项下,近期已有两场分别由不同企业发起的 EO 12866 行政审查会议申请。随着美国食品药品监督管理局(FDA)推进调味电子尼古丁传送系统(ENDS)上市前申请(PMTA)指南草案,该事项正成为行业关注的政策焦点。
目前该指南仍处于“通知阶段(Notice Stage)”。
两场会议、不同主体
根据公开记录:
2026年3月2日,分销企业 Breeze Smoke LLC 通过 Clark Hill Public Strategies 申请 EO 12866 会议(Meeting ID 1324024)。
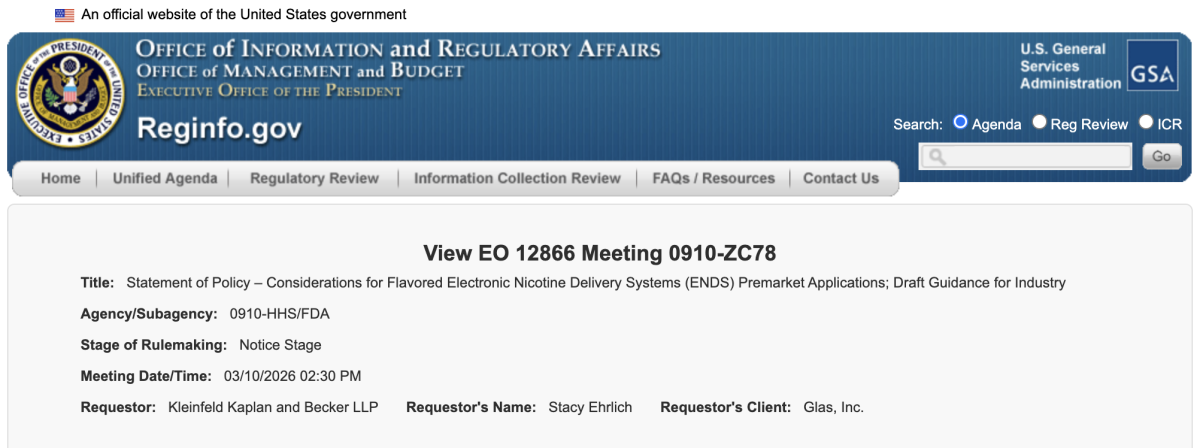
2026年3月10日(已安排),电子烟品牌及烟油制造商 Glas, Inc. 提出独立会议申请(Meeting ID 1329273),由 FDA 监管领域律所 Kleinfeld, Kaplan and Becker 合伙人 Stacy Ehrlich 代表陈述。
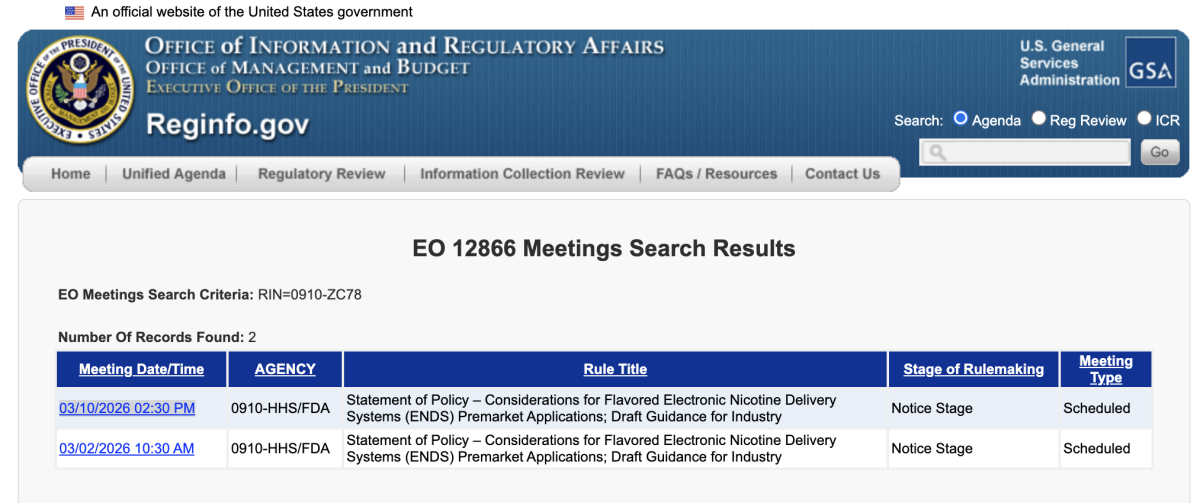
两家企业分别行动,但均围绕同一 RIN 编号提出审查请求,显示该指南草案可能影响分销与制造等不同层级市场主体。
政策焦点:RIN 0910-ZC78
RIN 0910-ZC78 全称为《调味电子尼古丁传送系统(ENDS)上市前申请指南草案》。
该文件属于行业指南(Guidance),并非正式规则(Rule),其目的在于进一步明确 FDA 在审查调味 ENDS 产品 PMTA 时的证据要求与评估框架。
根据《家庭吸烟预防与烟草控制法案》,FDA 在批准产品上市前必须认定其“有利于公众健康保护”(Appropriate for the Protection of Public Health,APPH)。在既往审查实践中,调味产品通常面临更高证据要求,需要提供产品特定及人群层面的数据,以证明其对成年烟民转化的潜在益处能够超过未成年人使用风险。
自2020年以来,FDA 已对绝大多数非烟草味 ENDS 产品发出营销拒绝令(MDO),授权案例主要集中于烟草味产品及少量设备平台。
企业影响与审批变量
Breeze Smoke 总部位于密歇根州 Hazel Park。根据《Crain’s Detroit Business》2025年9月11日报道,该公司2024年销售额约为 3.11亿美元。报道指出,在 FDA 于2025年加强对未经授权 ENDS 产品的执法行动(包括进口拦截及合规措施)后,该公司收入下降约 90%。
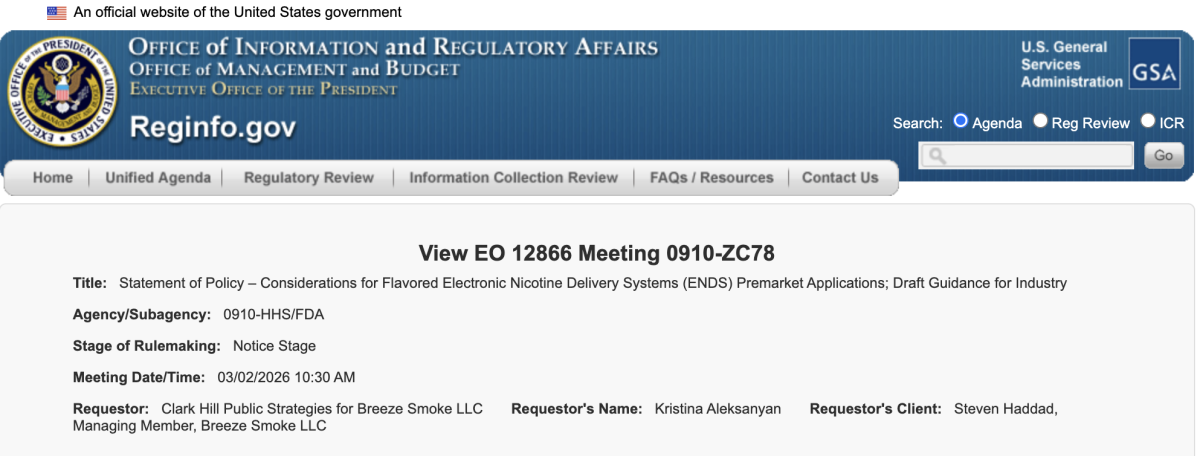
截至目前,Breeze 相关产品尚未获得 FDA 营销授权。
与此同时,处于 PMTA 审查流程中的企业亦对指南草案保持高度关注。
2Firsts 此前独家报道指出,FDA 官网后台曾出现疑似与 Glas 相关的状态更新,随后又被撤回。尽管 FDA 未就此作出说明,但相关变化一度引发市场对 Glas 审批进展的关注。

若 Glas 的申请确实进入关键审查阶段,则 RIN 0910-ZC78 指南中对调味产品证据标准的进一步明确,可能成为影响其审批路径的重要变量。
业内人士认为,Glas 聘请 Kleinfeld, Kaplan and Becker 参与 EO 12866 审查程序,属于对监管不确定性的风险管理安排,旨在确保 PMTA 审查标准在指南最终确定过程中保持一致性与可预期性。
EO 12866 监管程序背景
根据第12866号行政命令,重大监管行动在最终发布前通常需提交至白宫信息与监管事务办公室(OIRA)进行跨部门审查。
FDA 于 2026年2月18日 将该调味 ENDS 指南草案提交 OIRA 审查后,即进入行政审查阶段。在此期间,受影响的利益相关方可申请 EO 12866 会议,就监管分析方法、经济影响评估及政策一致性等问题陈述意见。
需要指出的是,指南(Guidance)不同于正式规则(Rule),其主要功能在于阐明机构对现行法规的解释及执行标准,而非直接创设新的法律义务。
OIRA 的职责在于评估监管行动的分析充分性与跨部门协调影响,并不替代 FDA 对 APPH 公共健康标准的科学判断。
结构性信号
在同一 RIN 编号下短期内出现多主体行政会议申请,反映出调味 ENDS 指南已成为当前美国烟草监管体系中的关键节点。
联邦监管持续强调未成年人使用风险控制;行业则关注成年烟民替代路径及审查标准的稳定性。不同层级企业在同一政策节点下采取行动,显示市场对监管可预期性的关注正在上升。
该指南最终文本的走向,或将进一步明确调味 ENDS 产品在 PMTA 框架下的现实授权边界。
后续观察
目前尚不明确 OIRA 是否会要求补充经济分析或提出修订建议。指南的最终发布时间仍有待观察。
2Firsts 将持续跟踪 RIN 0910-ZC78 的审查进展,以及其对美国调味 ENDS 市场结构与全球供应链可能产生的影响。
(封面图源:AI辅助)
关于全球电子烟产业的最新动态,欢迎继续关注2Firsts。

欢迎向 2Firsts 提供相关线索、投稿、联系访谈或针对本文发表评论。
请联系:info@2firsts.com,或在 LinkedIn 上联系两个至上 2Firsts CEO 赵童(Alan Zhao)。
声明
1. 本文仅供专业研究用途,聚焦行业、技术与政策等相关内容。文中涉及的品牌与产品,仅为客观描述之目的,不构成对任何品牌或产品的认可、推荐或宣传。
2. 含尼古丁产品(包括但不限于卷烟、电子烟、加热烟草、尼古丁袋)具有显著健康风险。使用者须遵守其所在辖区的相关法律法规。
3. 本文不应作为任何投资决策或相关建议的依据。对于内容中的任何错误或不准确之处,2Firsts不承担直接或间接责任。
4. 未达到法定年龄的个人禁止访问或阅读本文。
版权声明
本文为2Firsts原创内容,或转载自第三方来源并已明确标注出处。其版权及使用权归2Firsts或原始版权所有方所有。任何个人或机构未经授权,不得复制、转载、分发或以其他形式使用本文内容,违者将依法追究法律责任。
如有版权相关事宜,请联系:info@2firsts.com
AI辅助声明
本文部分内容可能借助AI工具完成翻译或编辑,以提升效率。但由于技术限制,可能存在误差。建议读者参考原始来源以获取更准确的信息。
欢迎读者指出可能存在的问题,请联系:info@2firsts.com




























